プレ・コロナの時代に、ちょと苦手な渋谷で焼鳥を食べたときのメモです。
-渋谷 森本 memo-
住所:渋谷区道玄坂2-7-4
-生酒 冷酒 (小瓶 300 ml) (増税前で1,239 JPY)- -RATING- ★★☆☆☆
-REVIEW-
銘柄は、生貯蔵酒 本醸造喜久水 生貯です(原材料:米(国産)・米麹(国産)・醸造アルコール;精米歩合:65%;日本酒度:+1.0前後;酸度:1.3前後;アリコール分:14%)。
ちなみに当時の定価は389円(税込)だったと思います。
清酒 喜久水 (619円)を冷やで注文したら、お店の人に「冷たいの?あったかいの?」と聞かれたので、「冷たいの」とこたえたら冷酒がきたです。カッコつけて「冷や」と言わず「常温で」と頼むべきでした。
-RATING- ★★★★★
-REVIEW-
塩味。粗挽きで肉々感リッチ(rich)。野趣的な風味で肉の旨味ふんだん。レモンの香味がついていて、食欲がより一層そそれられるいい匂い。文句なく旨い。
塩味。葱の焼き目の芳ばしい香り。弾力の強いフレッシュ(fresh)なモモ肉はとってもジューシー(juicy)。葱とモモ肉のコンボはやっぱり最強。
塩味。濃厚な旨味。歯に吸い付くような噛み心地が堪らなく気持ちいい。噛むほどに味が染み出して来るようで、真剣旨い。
-らっきょうワイン漬 (増税前で334 JPY)-ボタニカルリッチ(botanical rich)な香味で、フルーティー(fruity)ささえ感じる。ドギツい真っ赤な色合いとは裏腹に、けっこうマイルド(mild)な味わい。これ、相当旨いね。
塩味。なんとも中庸な食感が素晴らしい。肉の部分の味わいに深みがあって、かなり旨い。
ソフトタッチなレバの口溶けが最高に心地いい。レバ特有の野趣的な香味は穏やかながらしっかりあって丁度いい旨さ。
レバのうえにはぽん酢のジュレと刻み葱が載っている。ぽん酢ジュレはレバとしっかり絡んで相性抜群。ジュレの量が少なめなのが唯一の不満。
-ウイスキー (505 JPY)-
-REVIEW-
on the rocks。銘柄はサントリーの角。
このお店で熱燗をたのむと、電動式自動酒燗器からマイヤー(三角フラスコ)に一旦とった後コップに注がれるんだけど、ちょっと引くね。でも、焼き鳥は文句なしに旨かったです。
閑話休題
ハイ、また還元的アミノ化の総説的論文を読んでました。
そして、またまたアセトキシボロハイ(NaBH(OAc)3)推しです↓
A Review on the Use of Sodium Triacetoxyborohydride in the Reductive Amination of Ketones and Aldehydes
Org. Process Res. Dev., 2006, 10, 971-1031.
ジョンソン・エンド・ジョンソンの論文です。
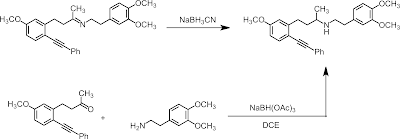
著者らが還元的アミノ化のREVIEWをまとめようと考えたきっかけの反応はこれです↓
合成しようとしていたのは薬剤候補化合物の前駆体で、最初はシアノボロハイ(NaBH3CN)を使うプロセスを考えていたそうですが、シアニドのコンタミがあり、簡便な方法では精製できない状況でした。そこで、アセトキシボロハイ(NaBH(OAc)3)を使ってみたら、当たり前だけどシアニドのコンタミ問題は解決し、収率も良好であることが分かりました。
この成果をもってアセトキシボロハイ(NaBH(OAc)3)に開眼した著者らは、この総説を執筆するに至ったのです。
まずは、この総説で紹介している一般的な反応条件(Reaction Conditions)のメモです↓
a) ケトンを用いたときのStandard Conditions:ketone (1 eq.), amine (1.05-1.1 eq.), AcOH (1 eq.), NaBH(OAc)3 (1.4 eq.) in DCE or THF as solvent at rt.
b) アルデヒドを用いたときのStandard Conditions:aldehyde (1 eq.), amine (1.05-1.1eq.), NaBH(OAc)3 (1.4 eq.) in DCE or THF as solvent at rt. (ケトンのときとの違いは、酢酸添加の有無だけ)
c) 1当量程度の弱酸やアミン塩を添加するのも有効で、最もよく使われるは酢酸です。
d) 強酸や強酸のアミン塩は、反応を完全に停止させてしまうかもしれず、基質にアミンの塩酸塩を使用する場合は、三級アミンを加えてフリーにしてやる必要がある。
e) ほとんどのケトンの還元的アミノ化では酢酸添加で反応が加速するが、そでも反応が遅い(> 24 hr)ケースでは、出発物質もしくは生成物のN-アセチル体またはN-エチル体が副生(GC:< 5%)する場合があるので心に留めておきましょう。
f) 酢酸の代わりにTFAを使うことで、N-アセチル化またはN-エチル化を回避できる。
g) の還元的アミノ化では、酢酸添加はまず必要ない。
h) アルデヒドと一級アミンとの反応でジアルキル化が問題となる場合、一級アミンを5%以上過剰に加えれば大抵改善する。
i) それ(h)でもダメなら、stepwise procedure (イミンを形成させた後に還元)。MeOH、THF、DCE溶媒中でイミン形成が速い。特にMeOHが速いのでオススメ。MeOH使ったときは、イミンのMeOH溶液をNaBH4で還元するとよい。
ほぼ前回メモったスタンダード・コンディションと同じです。やっぱadditiveでよく使うのは酢酸かTFAだよね。
ハイ、あとはひたすら実際の反応例の紹介になります。具体的には、
Reductive amination of saturated alicyclic and heterocyclic ketones : 49 examples
Diastereoselectivity in reductive amination of alicyclic ketones and bicyclic ketones : 23 examples
Reductive amination of saturated acyclic ketones : 18 examples
Reductive amination of aldehydes and primary amines : 94 examples
Reductive amination of aldehydes with secondary amines:119 examples
Use of formaldehyde in reductive amination:10 examples
Reductive amination of α- and β-keto acids/keto esters:13 examples
Reductive amination of γ- and δ-keto acids/keto esters:7 examples
Reductive amination of γ- and δ-amino acids/esters:6 examples
Reductive amination of substrates containing ketals and acetals:17 examples
Reductive amination of ketones and aldehydes with weakly basic amines:23 examples
Reductive aminations using solid supports:17 examples
Preparation of primary amines:7 examples
Miscellaneous reactions:17 examples
Limitations:15 examples
の全約435例がTableにまとめられています(沢山あります)。
まずは、キラルな環状ケトンを基質に使ったときのジアステレオ選択性の例です。基本、ヒドリド試薬は立体障害の最も小さい方がら接近していくので、新たに形成するC-N結合は基本cis (syn)体がメインになる傾向にあります。それでも世の中広いので、選択性が全くでないものから、中程度、エクセレントな選択性を示すものまで色取り取りです。
cis-N-benzyl-3-methylamino-4-meythylpiperidine(直上スキーム最後)の合成は25 kgスケールで実施していて、普通のボロハイ(NaBH4)と酢酸からin situでアセトキシボロハイ(NaBH(OAc)3)を調製しています。中間体のイミンはトルエン/THF/EtOHの混合溶媒中で調製され、イミン溶液をアセトキシボロハイの懸濁液中に加えていくという、プロセス仕様(っていうか、お釜使ってるよね)の合成法で造っています(Org. Process Res. Dev., 2003, 7, 115.)。
もう一つ実用的な合成例(4モルスケール)がこちら↓
Chirality, 2005, 17, S149.
一段階目の還元的アミノ化は水酸基が配向基となってtrans-体が優勢となります。DCE中室温下アセトキシボロハイ(NaBH(OAc)3)で還元するとtrans:cis=1.9:1ですが、D-バリンのtert-ブチルエステルの量を増やし、CH3CN中50˚Cで反応を反応させることにより選択性が7:1に向上します。さらに、還元剤にボロハイ(NaBH4)とプロピオン酸からin situで調製したSodium Tripropoxyborohyrideを用いて70˚Cで還元すると選択性がさらに高まります(trans:cis=10:1)。
続きです↓
あと(おきまりですが)、よりデカいアシルオキシ基の"ボロハイ"で選択性が高いです。
あと、(総説の)著者らも推してる興味深い例です↓
安定なオゾニドアルデヒドの還元的アミノ化↓
Reductive Amination of Ozonide Aldehyde
J. Org. Chem., 2004, 69, 6470.
ジアルデヒドとジアミンの還元的重縮合なんていうのもあります↓
Reductiove Condensation of Dialdehyde and Diamine
Polym. J. (Tokyo), 1998, 30, 857.
この反応はLiClの添加がキモで、それによって収率が大きく改善します。(元文献の)著者らは中間体のヒドロキシルアミンの水素結合を開裂させイミニウムイオンの形成を促進する効果があるのではなかろうかと想像しています。ちなみに、AcOHの添加や加熱(70℃)、冷却(5℃)は反応改善の効果はありません。あと、Ti(Oi-Pr)4/NaBH4, Cl3SiH/DMF, ボラン-ピリジン錯体では全然ダメです。
溶媒にDMAC (N,N-dimethylacetamide)を使用した例です↓
4.4モルスケールで実施しています。DMF溶媒だと二級アミンがホルミル化されるという副反応が起こりますが、DMAC溶媒では改善されます(
Org. Process. Res. Dev.,
2005,
9, 490.)。
α-ケトエステルはエステルの電子吸引性によりケト基が活性化されていて、還元的アミノ化を促進しますが、それと同時にケトンも還元されやすくなるので、目的の還元的アミノ化の反応速度が遅い場合は注意が必要です。
β-ケトエステルの還元的アミノ化はちょっと特殊で、はじめに形成する中間体はイミンではなくエナミンなんだそうです。
γ-ケトエステルとδ-ケトエステルは、アルキル鎖がいい感じの長さになるので、反応条件下で環化してラクタムを形成します。"reductive ractamization"って言うそうです。
ということで、γ-およびδ-アミノ酸(エステル)の還元的アルキル化においても、反応条件下で環化してラクタムまでいっちゃいます。
スルホンアミドを使った還元的アミノ化は、相手のカルボニル化合物がアルデヒドなら脂肪族でも芳香族でもイケイケですが、ケトンだとダメダメだそうです。
アセトキシボロハイ(NaBH(OAc)
3)は樹脂(Solid Support)に付きのカルボニル化合物(ケトン、アルデヒド)やアミンとの還元的アミノ化(アルキル化)にも適用可能で、BAL、BAL-PEG-PS、FMPB、FBMP、HMBA-POEPOP900、Merrifield、PEG-OMe、PS-Trityl-Cl、Rink、Rink Amide、Wang、4-(4-formyl-3-methoxyphenoxy)butyric resinといった樹脂がcompatibleです(オイラ、レジンは全然分かんないけど)。
あと、トリアセトキシボロハイドライドが樹脂(MP resin)にくっついた試薬もあるんですね。MP-BH(OAc)
3)っていう試薬です。
Tetrahedron Lett., 2003, 44, 4957.
この試薬をジャブ程度に使ったことがあるんだけど、反応の進行が遅いと思いましたね。まあでも、後処理は楽です。スカベンジャーレジンを加えて濾過するだけなんで。
それから1級アミンの合成法です。よく用いられるアミンソースはアンモニアと酢酸アンモニウムで、還元剤としてはシアノボロハイ(NaBH3CN)が有効です。何故なら、アンモニアや酢酸アンモニウムがよく溶けるメタノール中での反応が普通に可能であるためです(シアノボロハイの加溶媒分解速度は十分に遅い)。酢酸アンモニウムのDCE, THF, CH3CNへの溶解度が小さいため、アセトキシボロハイ(NaBH(OAc)3)の使用は厳しく、10 eq.の酢酸アンモニウムを使用してもジアルキル化が進行してしまいます。
(アンモニアガスを吹き込んで、アンモニア溶液を調製して反応を行えばいいかもだけど、実験室では面倒だよね)
それでも著者らは鋭意検討して、トリフルオロ酢酸アンモニウムならTHFに十分に溶解するので、アセトキシボロハイ(NaBH(OAc)3)を用いた還元的アミノ化に使えることを見出しました。
Abdel-Magid, A. F.; Maryanoff, C. A. Use of Sodium Triacetoxyborohydride in Reductive Amination of Ketones and Aldehydes. In Reductions in Organic Synthesis: Recent Advances and Practical Applications; Abdel-Magid, A. F., Ed.; ACS Symp. Ser. 641; American Chemical Society: Washington DC, 1996; p 201.
他のグループからの報告(特許)もあります↓
U.S. Patent Application 04/0224954A1, 2004.
さて、けっこうメモッてきましたが、最後にアセトキシボロハイ(NaBH(OAc)3)を使った還元的アミノ化のスタンダードコンディションの限界(15 examples)をメモってフィニッシュしましょう↓
やはりネックとなるのは芳香族ケトンやα,β-不飽和ケトンや嵩高い立体障害の大きい反応性の低いケトンとの反応です。
アセトフェノンとベンジルアミンとの反応では、10日間反応させてやっと収率55%です。
アセトフェノンとシクロヘキシルアミンとの反応や、1-アセチルシクロヘキセンとモルホリンの反応も遅いです。
ベンジルアミンとの競合反応では、やはり反応性の高い飽和のケトンとの反応が効率的に進行し、活性の低い芳香族ケトンやα,β-不飽和ケトンは原料回収に終わります。
それから、立体的に嵩高いアミン(ジイソプロピルアミン)やケトン(カンファー)は還元的アミノ化が苦手です(基本、嵩高い化合物は反応性低めだよね)。
2,4,6-トリクロロアニリンや2,4-ジブロモアニリンといった非常に塩基性の弱いアミンでケトンとの反応は厳しいです。
イミノスチルベンはヘキサナールと反応しますが、そのジヒドロ体であるイミノジベンジルは活性を示しません。
[60]フレロピロリジンは非常に塩基性が弱い化合物ということで、全然ダメです。
ベンズアルデヒドとフェニルヒドラジンとの反応では、生成するヒドラゾンが安定で還元されません。
同様にオキシムも還元されません。
前述したようにベンズアルデヒドとスルホンアミドは反応するけど、カルボキサミド程度ではノーリアクションです。
ハイ、ここまで徒然なるままに反応例をメモってきましたが、ボク的にこの総説を一言で締めくくると、
1級アミンの還元的アミノ化による合成は、トリフルオロ酢酸アンモニウムつかうとイイよ
以上、国内二流大出のテクニシャン(研究補助員)の還元的アミノ化入門メモでした。